NGHIÊN CỨU TỔNG HỢP VÀ KHẢO SÁT CÁC YẾU TỐ ẢNH HƯỞNG TỚI KHẢ NĂNG HẤP PHỤ 2,4-DICLOPHENOXYACETIC AXIT CỦA VẬT LIỆU CACBON AEROGEL/Fe3O4
Phân viện Hóa - Môi trường, Trung tâm Nhiệt đới Việt - Nga
Số 63 Nguyễn Văn Huyên, Nghĩa Đô, Cầu Giấy, Hà Nội
Số điện thoại: 0986089801; Email: ntthuhang2501@gmail.com
Nội dung chính của bài viết
Tóm tắt (Abstract)
STUDY ON SYNTHESIS AND SURVEY EFFECTS OF FACTORS TO ABILITY ADSORPTION 2,4-D OF COMPOSITE MATERIALS OF CARBON AEROGEL/Fe3O4
In this study, materials graphene oxide (GO), magnetite nanoparticles (Fe3O4), carbon aerogel (CA), composite of carbon aerogel/Fe3O4 (CA/Fe3O4) were prepared success. Materials were chacracterized by X-ray diffraction (XRD), fourier transform infrared spectroscopy (FTIR) and field emission scanning electron microscopy/energy dispersive X-ray spectroscopy (FESEM/EDX). The obtained results show that the Fe3O4 have a cubic crystal structure and have a nanoparticle's size (50-100 nm); the nano Fe3O4 were well dispersed with the carbon aerogel to form the composite materials of CA/Fe3O4. The effects of initial 2,4-D concentrations, contact time, pH values on the 2,4-D adsorption were investigated from batch tests. The experimental data were analyzed by Langmuir, Freundlich models of adsorption. The 2,4-D adsorption on the material was fitted to Freundlich isotherm and the maximum adsorption capacity was found to be 102.04 mg/g.
Từ khóa (Keywords)
Carbon aerogel, aerogel, graphene oxide, adsorption, cacbon aerogel, graphen oxit, Hấp phụ, 2, 4-D
Chi tiết bài viết
1. ĐẶT VẤN ĐỀ
Nước là nguồn sống cho con người. Thế nhưng, chính con người đã có những tác động làm hủy hoại sự trong sạch của môi trường nước. Tình trạng ô nhiễm nước không chỉ xảy ra ở Việt Nam mà còn xảy ra ở mọi quốc gia trên thế giới. Nguyên nhân chủ yếu là từ chất có trong thuốc bảo vệ thực vật, chất thải công nghiệp chưa được xử lý, rác thải sinh hoạt,…
Để loại bỏ các chất ô nhiễm trong môi trường nước người ta có thể sử dụng nhiều phương pháp khác nhau như: sử dụng vật liệu hấp phụ [1, 13-15], vật liệu quang xúc tác [2], hệ oxy hóa tiên tiến [3],... Các kết quả nghiên cứu đều cho thấy khả năng xử lý khá tốt, tuy nhiên vẫn còn tồn tại những nhược điểm như năng lượng cung cấp lớn, hóa chất sử dụng nhiều dẫn đến những khó khăn trong việc kiểm soát và xử lý triệt để các chất ô nhiễm trong nước thải, khó khăn trong việc thu hồi tái sử dụng vật liệu. Do vậy, việc tìm ra một loại vật liệu mới tiên tiến vừa có hiệu quả xử lý chất ô nhiễm tốt, quy trình tổng hợp đơn giản, hiệu suất xử lý cao, chi phí thấp không gây ô nhiễm thứ cấp, thu hồi dễ dàng là yêu cầu cấp thiết để có thể đáp ứng được nhu cầu thực tiễn. Vật liệu cacbon aerogel/Fe3O4 là loại vật liệu đang được nhiều nhà khoa học trong và ngoài nước quan tâm, nghiên cứu do có khả năng kết hợp nhiều đặc tính của các thành phần, qua đó nâng cao hiệu quả xử lý của vật liệu [4].
Với những ưu điểm trên, chúng tôi đã tiến hành nghiên cứu chế tạo vật liệu cacbon aerogel/Fe3O4 và khảo sát các yếu tố ảnh hưởng đến khả năng xử lý của vật liệu với tác nhân ô nhiễm môi trường lựa chọn là 2,4-Diclophenoxyacetic axit (2,4-D).
2. THỰC NGHIỆM
2.1. Hóa chất
Hóa chất và vật liệu sử dụng bao gồm: Graphit 99,5%, kích thước vảy < 50 µm (Đức), H2SO4 95-97% (Đức), HCl 37% (Đức), KMnO4 99,5% (Trung Quốc), 2,4-Diclophenoxyacetic axit 98% (CIL), FeCl3.6H2O 99,0% (Trung Quốc), FeCl2.4H2O 98,0% (Trung Quốc), C6H6O8 99,0-110,5% (Đức), H2O2 30% (Trung Quốc), NaOH 99,0% (Đức).
2.2. Quy trình tổng hợp graphen oxit
Graphen oxit (GO) được tổng hợp từ graphit dựa theo phương pháp Hummer cải tiến như sau: 3 g bột graphit được thêm vào 42 mL H2SO4 đặc làm lạnh từ 0-5℃ và khuấy liên tục trong 30 phút, thêm từ từ 0,45 g KMnO4 vào hỗn hợp phản ứng, khuấy liên tục 15 phút. Sau đó thêm 9 g KMnO4 vào hỗn hợp, duy trì nhiệt độ không quá 35℃ tiếp tục khuấy trong 30 phút, nước cất được thêm từ từ vào hỗn hợp, nhiệt độ hệ được duy trì không quá 50℃, tiếp tục khuấy trong 1 giờ. 10,5 ml H2O2 30% được thêm vào để loại bỏ pemanganat và mangan dioxit còn lại sau phản ứng, sau đó sản phẩm được lọc rửa với axit HCl loãng và nước cất đến pH = 7. Sản phẩm được sấy khô ở 60℃ trong chân không, hỗn hợp đã sấy khô được nghiền mịn bằng cối đá mã não và bảo quản trong bình kín [5].
2.3. Quy trình tổng hợp nano oxit sắt từ
Các hạt nano oxit sắt từ (Fe3O4) được tổng hợp bằng phương pháp đồng kết tủa. Pha 150mL hỗn hợp dung dịch FeCl3.6H2O và FeCl2.4H2O với tỷ lệ mol là 1:1. Sau đó, dung dịch NaOH được nhỏ từ từ vào hỗn hợp trong điều kiện khuấy liên tục (pH~12). Khi phản ứng kết thúc rửa kết tủa bằng nước cất, etanol tới khi pH = 7, lọc sấy kết tủa ở 60oC trong 12 giờ [6].
2.4. Quy trình tổng hợp cacbon aerogel
20 mL huyền phù GO với nồng độ 8 mg/mL được siêu âm trong 30 phút để tạo hỗn hợp đồng nhất. Sau đó, thêm chất khử vào hệ (đồng thời siêu âm), đậy kín nắp. Tiến hành gia nhiệt lên 90°C trong 6 giờ để hình thành graphen hydrogel (GH). Sau đó, mẫu GH được lấy ra và ngâm với hỗn hợp etanol/nước với tỷ lệ 1/3, thay hỗn hợp etanol/nước thường xuyên để loại bỏ các tạp chất còn lại. Mẫu GH bảo quản lạnh -30oC trong 6h, sau đó đem đi sấy thăng hoa trong 48 giờ thu được cacbon aerogel [7].
2.5. Quy trình tổng hợp cacbon aerogel/Fe3O4
GO (hàm lượng 8 mg/mL) được phân tán vào hỗn hợp dung dịch FeCl3.6H2O và FeCl2.4H2O với tỷ lệ mol là 1:1. Nhỏ từ từ dung dịch NaOH vào hỗn hợp huyền phù trong điều kiện khuấy liên tục (pH~10). Tiếp theo, chất khử axit ascorbic được cho vào hỗn hợp, siêu âm 15 phút. Chuyển hỗn hợp vào bình thủy nhiệt, gia nhiệt ở 90°C trong 6 giờ để hình thành graphen hydrogel/Fe3O4 (GH/Fe3O4). Mẫu GH/Fe3O4 bảo quản lạnh -30oC trong 6h. Sau đó được sấy đông khô -50oC trong 48 giờ thu được vật liệu cacbon aerogel/Fe3O4 (CA/Fe3O4).
2.6. Phương pháp phân tích
Các phương pháp phân tích hình thái bề mặt vật liệu và đặc trưng cấu trúc được sử dụng gồm: Kính hiển vi điện tử quét SEM (Jeol - Nhật Bản, SM - 6510LV), tán xạ năng lượng EDX (Oxford Instrument-Anh, X-Act), phổ hồng ngoại FTIR (Thermo Scientific - Mỹ, Nicolet iS10) được thực hiện tại Viện Kỹ thuật Nhiệt đới/Viện Hàm Lâm Khoa học và Công nghệ Việt Nam; phổ nhiễu xạ Rơnghen XRD (Bruker - Đức, D8 ADVANCE) được thực hiện tại Bộ môn Hóa học Vô cơ/ Khoa Hóa/ Đại học Khoa học Tự nhiên/ Đại học Quốc gia Hà Nội.
Trong nghiên cứu, nồng độ 2,4-D được xác định theo phương pháp sắc ký lỏng hiệu năng cao (High - performance liquid chromatography - HPLC) 6340 Triple Quad LC/MS tại Phân viện Hóa - Môi trường, Trung tâm Nhiệt đới Việt - Nga: Cột Zobrax Eclipse plus C18 2,1 x 50 mm; 1,8 µm; Dung môi pha động A: axit acetic 0,05%, B: acetonitrile; Tốc độ dòng 0,26 ml/phút.
2.7. Phương pháp thử nghiệm khả năng hấp phụ 2,4-D của CA/Fe3O4
Một lượng 0,02 g vật liệu hấp phụ được phân tán đều với 20 mL dung dịch 2,4-D có nồng độ Co (mg/L), sau đó lắc đều trên máy lắc với tốc độ 160 vòng/phút - trong khoảng thời gian t (phút). Các hạt vật liệu được tách ra khỏi dung dịch bằng nam châm, dung dịch còn lại được lọc qua giấy lọc băng xanh. Nồng độ 2,4-D trong dung dịch Ce (mg/L) được xác định trên thiết bị sắc ký lỏng hiệu năng cao LC/MS.
3. KẾT QUẢ VÀ THẢO LUẬN
3.1. Hình ảnh bề mặt và đặc trưng cấu trúc của vật liệu chế tạo
3.1.1. Hình ảnh các vật liệu chế tạo GO, CA, Fe3O4, CA/Fe3O4
Hình 1 là ảnh chụp SEM của mẫu vật liệu GO, CA, Fe3O4, CA/Fe3O4 ở độ phân giải cao. Có thể thấy các hạt Fe3O4 với kích thước ~50-100 nm, hình dạng hình cầu, đồng nhất Hình 1c. Trong khi đó, vật liệu CA/Fe3O4 có kích thước hạt 10 µm. CA hình ảnh bề mặt nhiều lỗ trống và xốp Hình 1b. Có thể giả định theo quy trình chế tạo vật liệu nêu trên, các hạt nano Fe3O4 được phân tán đồng đều và lần lượt được bao bọc bởi các rGO, là cơ sở minh chứng cho kết quả đặc trưng từ tính của vật liệu đã chỉ ra trên Hình 1d và phù hợp với kết quả phân tích thành phần nguyên tố bằng EDX trên Hình 2 với sự xuất hiện của các nguyên tố C, O, Fe trên hình ảnh phổ.

Hình 1. Hình ảnh bề mặt các vật liệu a) GO, b) CA, c) Fe3O4, d) CA/Fe3O4
thông qua kính hiển vi điện tử quét SEM
3.1.2. Giản đồ nhiễu xạ Rơnghen
Hình 2 cho thấy kết quả phân tích nhiễu xạ tia X của các vật liệu tổng hợp được. Đỉnh nhiễu xạ nhọn (002) ở 2θ = 9,98o tương ứng với GO [8, 9]. Sau quá trình khử hóa học bằng axit ascorbic, đỉnh (002) của GO không xuất hiện trong khi một đỉnh rộng khác khoảng 24,6o xuất hiện. Sự không xuất hiện của đỉnh nhọn khoảng 10o có thể là do sự bong tróc của cấu trúc phân lớp của graphit oxit. Đỉnh rộng ở khoảng 24,6o có thể được gây ra bởi sự sắp xếp lại một phần của các lớp graphen đã tách lớp để tạo thành cấu trúc tinh thể [8, 10].
Giản đồ XRD của mẫu Fe3O4 biểu thị rõ 6 đỉnh đặc trưng ở các giá trị 2θ là 30, 35, 43, 53, 57 và 62 tương ứng với các mặt phẳng tinh thể (220), (311), (400), (422), (511) và (440). Đặc điểm này đồng nghĩa với việc tổng hợp thành công nano oxit sắt từ [11, 12]. Và giản đồ XRD của vật liệu CA/Fe3O4 biểu thị rõ các đặc điểm của cả CA và Fe3O4.
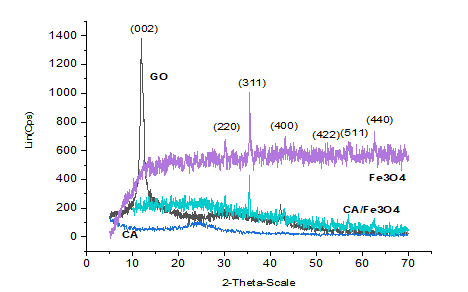
Hình 2. Giản đồ nhiễu xạ XRD của vật liệu GO, Fe3O4, CA, CA/Fe3O4
3.1.3. Phổ hồng ngoại FTIR
Các mẫu đặc trưng bởi phổ hồng ngoại FT-IR thể hiện ở Hình 3 là các phổ tương ứng của GO, CA, Fe3O4, CA/Fe3O4. Trong vùng 4000-400 cm-1 có thể được cho là nhóm O-H [10]. Các cực đại hấp phụ ở 1720 cm-1 tương ứng với các nhóm chức carbonyl nằm ở rìa của các tấm GO (COOH và C=O) [9]. Trong khi cực đại ở 1620 cm-1 được cho là các dao động C=C của khung graphen. Dao động C-O trong các nhóm hydroxyl hoặc epoxy được quan sát thấy ở 1410 cm-1 và 1060 cm-1. Một điểm cần lưu ý rằng tất cả các cường độ cực đại tại các dao động của các nhóm chức oxy trong CA đều giảm so với cường độ trong GO. Điều này cho thấy việc khử thành công GO bằng axit ascorbic nhưng quá trình khử không hoàn toàn. Riêng với phổ FT-IR của Fe3O4 dao động đặc trưng ở khoảng 590 cm-1 đó là dao động Fe-O của Fe3O4.
Đối với CA/Fe3O4, cường độ của các nhóm chứa oxy giảm, cho thấy GO đã khử một phần tạo rGO. Đồng thời, hạt nano sắt từ đã liên kết với cấu trúc GA với sự xuất hiện của nhóm Fe-O tại 590 cm-1.
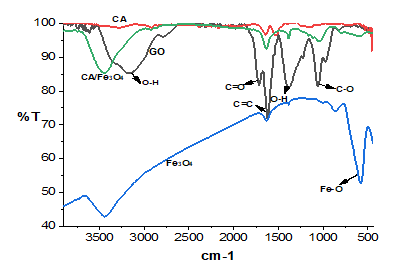
Hình 3. Phổ FTIR của vật liệu GO, CA, Fe3O4, CA/Fe3O4
3.1.4. Xác định thành phần các nguyên tố trong vật liệu CA/Fe3O4
Thành phần các nguyên tố có trong các vật liệu tổng hợp được, được thể hiện tại Hình 4.
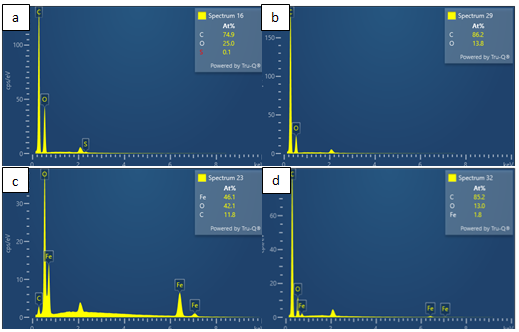
Hình 4. Giản đồ phân tích EDX của mẫu a) GO, b) CA, c) Fe3O4, d) CA/Fe3O4
Phổ EDX của GO, CA được thể hiện trong Hình 4a và Hình 4b. Chỉ có sự hiện diện của các nguyên tố C và O trong GO và CA, cho thấy độ tinh khiết cao hoặc không có nguồn tạp chất đáng kể đối với các sản phẩm thu được (<0,5% - Giới hạn định lượng kỹ thuật EDX). Trong quá trình khử có dẫn đến giảm phần trăm nguyên tử oxi trên bề mặt từ 25,0% (trong GO) xuống 13,0% (trong CA), nhưng lại tăng tỷ lệ C/O từ 3,0 (trong GO) lên 6,25 (trong CA). Điều này chứng tỏ đã khử thành công các nhóm chức oxi (-OH, -O-, -C=O và -COOH).
Phổ EDX của Fe3O4 được thể hiện trong Hình 4c. Dữ liệu cho thấy sự có mặt của hai nguyên tố Fe và O. Ngoài ra còn có sự xuất hiện của nguyên tố C khoảng 11,8% điều này được giải thích là do trong quá trình rửa vật liệu bằng etanol đã xảy ra sự hấp phụ etanol trên bề mặt vật liệu Fe3O4. Trung bình % trọng lượng của Fe và O lần lượt là 46,1 và 42,1. Hình 4d là phổ EDX của vật liệu CA/Fe3O4 trong đó thành phần các nguyên tố chỉ có C, O và Fe cho thấy độ tinh khiết cao và không có tạp chất. Trong đó trung bình % trọng lượng của các nguyên tố C, O và Fe lần lượt là 85,2; 13,0 và 1,8. Như vậy các hạt nano Fe3O4 đã được phân tán trên bề mặt của vật liệu cacbon aerogel. Quá trình khử cũng đã diễn ra do phần trăm nguyên tử O bị giảm trên bề mặt của vật liệu.
3.2. Kết quả nghiên cứu các yếu tố ảnh hưởng đến khả năng hấp phụ của vật liệu CA/Fe3O4
3.2.1. Ảnh hưởng nồng độ 2,4-D
Tiến hành khảo sát hấp phụ 20 mL dung dịch 2,4-D với 0,02 g CA/Fe3O4 tại các nồng độ của 2,4-D lần lượt là 10, 30, 50, 70, 90, 110, 130 và 150 mg/L. Kết quả sự ảnh hưởng của nồng độ 2,4-D đến khả năng hấp phụ của vật liệu CA/Fe3O4 được thể hiện trên Hình 5.
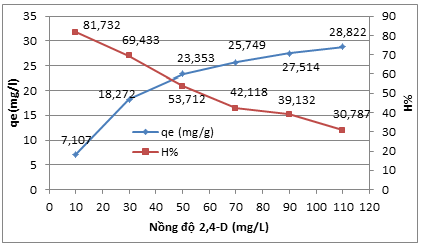
Hình 5. Sự ảnh hưởng của nồng độ 2,4-D đến hiệu suất và dung lượng hấp phụ
Hình 5 cho thấy đối với dung dịch có nồng độ 2,4-D từ 10 đến 30 mg/L thì hiệu suất hấp phụ cao và dung lượng hấp phụ tăng nhanh. Điều này có thể giải thích là do ban đầu bề mặt và các mao quản đang còn trống, diện tích bề mặt bị chiếm rất nhỏ, phân tử 2,4-D dễ dàng xâm nhập và hình thành các liên kết.
Khi diện tích bề mặt bị chiếm đủ lớn thì quá trình hấp phụ diễn ra chậm và có chiều hướng tăng chậm, khi nồng độ 2,4-D từ 50 mg/L đến 130 mg/L hiệu suất hấp phụ giảm dần và dung lượng hấp phụ tăng không đáng kể.
3.2.2. Thời gian cân bằng
Theo khảo sát sơ bộ ban đầu dung lượng hấp phụ cực đại của vật liệu khá tốt đạt 102,04 mg/g. Do vậy, chúng tôi tiến hành hấp phụ 20 mL dung dịch 2,4-D tại nồng độ 100 mg/L với 0,02 g vật liệu CA/Fe3O4 lắc tại các khoảng thời gian 30, 60, 120, 150, 180, 210, 240 và 300 phút. Kết quả thu được như trong Hình 6.
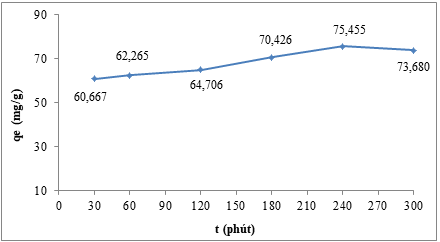
Hình 6. Tải trọng hấp phụ của vật liệu CA/Fe3O4 tại các khoảng thời gian khác nhau
Kết quả cho thấy tải trọng hấp phụ của vật liệu CA/Fe3O4 cao nhất (75,46 mg/g) tại khoảng thời gian là 240 phút.
3.2.3. Ảnh hưởng của pH
pH của một dung dịch nói chung đóng một vai trò quan trọng trong phản ứng hóa lý ở bề mặt phân cách nước - rắn.
Ảnh hưởng của pH đến khả năng hấp phụ 2,4-D được nghiên cứu với 0,02 g vật liệu CA/Fe3O4 hấp phụ 20 mL dung dịch 2,4-D 50 mg/L ứng với các giá trị pH thay đổi: 3, 4, 5, 6, 7, 8, 10. Kết quả được thể hiện trong Hình 7.
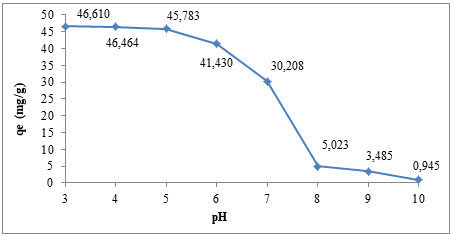
Hình 7. Ảnh hưởng của pH đến khả năng hấp phụ của CA/Fe3O4
Từ kết quả cho thấy vật liệu có dung lượng hấp phụ tốt trong môi trường axit khoảng pH từ 3-5 và gần như không hấp phụ 2,4-D trong môi trường kiềm khoảng pH ≥ 8. Nguyên nhân môi trường có tính kiềm bề mặt vật liệu sẽ tích điện âm ảnh hưởng bất lợi đến sự hấp phụ 2,4-D của CA/Fe3O4. Trong khoảng pH < 7 bề mặt vật liệu sẽ tích điện dương, 2,4-D tồn tại chủ yếu ở dạng ion nên có lợi cho sự hấp phụ. Ngoài ra trong môi trường kiềm còn có sự cạnh tranh hấp phụ của OH- nên khả năng hấp phụ của vật liệu giảm đi.
3.2.4. Khảo sát đẳng nhiệt hấp phụ trên vật liệu CA/Fe3O4
Hình 8, Hình 9 là các hình biểu diễn phương trình dạng tuyến tính của 2 mô hình đẳng nhiệt hấp phụ Langmuir, Freundlich.
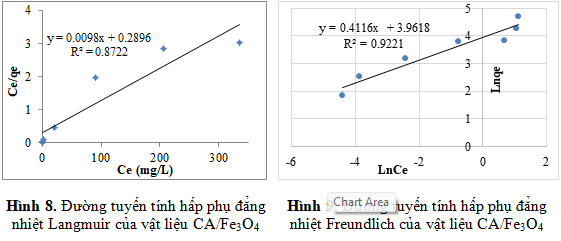
Bảng 1. Thông số các mô hình hấp phụ 2,4-D đối với vật liệu CA/Fe3O4

Từ Bảng 1 nhận thấy Kf = 52,55 và 1/n = 0,4116. Giá trị KF cũng cho thấy vật liệu CA/Fe3O4 có khả năng hấp phụ lớn 2,4-D, giá trị 1/n nhỏ chứng tỏ bản chất quá trình hấp phụ là tương tác hóa học.
Từ giá trị hệ số hồi quy R2 thu được đối với các đường đẳng nhiệt Langmuir, Freundlich cho thấy mô hình hấp phụ đẳng nhiệt Freundlich thích hợp hơn so với mô hình Langmuir. Điều này có nghĩa là bề mặt của vật liệu hấp phụ có lỗ xốp, hấp phụ xảy ra trên bề mặt vật liệu; giá trị n > 1 trong phương trình Freundlich chỉ ra rằng quá trình hấp phụ diễn ra thuận lợi. Dung lượng hấp phụ cực đại của vật liệu CA/Fe3O4 đối với 2,4-D đạt 102,04 mg/g cao hơn gấp 7,7 lần và 13,3 lần so với khi sử dụng vật liệu hydroxyapatit và composit IONPsHAp [13]. Gấp 361,2 lần và 1,7 lần so với khi sử dụng than hoạt tính dạng hạt biến tính [14] và nanocomposit than hoạt tính từ tảo [15].
4. KẾT LUẬN
Trong nghiên cứu này, các loại vật liệu GO, nano oxit sắt từ, cacbon aerogel và cacbon aerogel/oxit sắt từ đã được điều chế thành công. Kết quả phân tích thành phần cấu trúc cho thấy các hạt nano oxit sắt từ có hình thái đồng nhất, kích thước hạt trung bình khoảng 50-100 nm, phân tán tốt trong vật liệu cacbon aerogel. Nghiên cứu khảo sát các yếu tố ảnh hưởng đến khả năng hấp phụ của vật liệu cacbon aerogel/Fe3O4 với việc loại bỏ 2,4-D trong nước, kết quả chỉ ra rằng vật liệu CA/Fe3O4 có dung lượng và hiệu suất hấp phụ 2,4-D tăng nhanh ở khoảng nồng độ ≤ 50 mg/L, giảm dần khi nồng độ 2,4-D > 50 mg/L, khoảng pH tối ưu là 4-5, thời gian cân bằng 240 phút, các số liệu thí nghiệm thu được phù hợp với mô hình lý thuyết hấp phụ đẳng nhiệt Freundlich, dung lượng hấp phụ cực đại 102,04 mg/g.
Tài liệu tham khảo
2. Hoàng Hiệp, Lê Thanh Sơn, Hiệu quả quang xúc tác phân hủy nước ô nhiễm 2,4,5-T trên vật xúc tác quang Cu/TiO2 và Fe/TiO2 - và động học phản ứng, Tạp chí phân tích Hóa, Lý và Sinh học, 2015, 20(1):106-110.
3. Nguyễn Ngọc Tiến, Lâm Vĩnh Ánh, Đào Thế Hữu, Nghiên cứu đánh giá hiệu quả xử lý 2,4-D, 2,4,5-T trong dung dịch sau rửa giải đất nhiễm da cam dioxin bằng một số hệ oxy hóa tiên tiến, Tạp chí Phân tích Hóa, Lý và Sinh học, 2015, 20(2):109-115.
4. Nguyễn Văn Nội, Vật liệu ứng dụng trong xử lý môi trường, NXB. Đại học Quốc gia Hà Nội, 2017.
5. Cao Phương Anh, Hán Duy Linh, Vũ Minh Châu, Nguyễn Thị Thu Hằng, Nghiên cứu tổng hợp và khảo sát khả năng xử lý xanh methylene và đỏ công gô trong môi trường nước của vật liệu composit từ tính oxit sắt/graphen oxit, Tạp chí Khoa học và Công nghệ nhiệt đới, 2022, 28:22-29.
6. Poedji Loekitowati Hariani, Muhammad Faizal, Ridwan, Marsi, and Dedi Setiabudidaya, Synthesis and Properties of Fe3O4 Nanoparticles by Co-precipitation Method to Removal Procion Dye, International Journal of Environmental Science and Development, 2013, 4(3):336-340.
7. Nguyễn Thị Lan, Tổng hợp vật liệu graphen aerogel để hấp phụ chất màu hữu cơ, Báo cáo luận văn thạc sĩ, 2018.
8. L. Stobinski, B. Lesiaka, A. Malolepszy, M. Mazurkiewicz, B. Mierzwa, J. Zemek, P. Jiricek, I. Bieloshapka, Graphene oxide and reduced graphene oxide studied by the XRD, TEM and electron spectroscopy methods, Journal of Electron Spectroscopy and Related Phenomena, 2014, 195:145-154.
9. Sasha Stankovich, Dmitriy A. Dikin, Richard D. Piner, Kevin A. Kohlhaas, Alfred Kleinhammes, Yuanyuan Jia, Yue Wu, Son Binh T. Nguyen, Rodney S. Ruoff, Synthesis of graphene-based nanosheets via chemical reduction of exfoliated graphite oxide, Carbon, 2007, 45:1558-1565.
10. Tarko Fentaw Emiru, Delele Worku Ayele, Controlled synthesis, characterization and reduction of graphene oxide: A convenient method for large scale production, Egyptian Journal of Basic and Applied Sciences, 2016.
11. M. S. Raghua, K. Yogesh Kumar, M. K. Prashanth, B. P. Prasanna, Raj Vinuth, C. B. Pradeep Kumar, Adsorption and antimicrobial studies of chemically bonded magnetic graphene oxide-Fe3O4 nanocomposite for water purification, Journal of Water Process Engineering, 2017, 17:22-31.
12. Jian Lu, Yi Zhou, Juying Lei, Zhimin Ao, Yanbo Zhou, Fe3O4/graphene aerogels: A stable and efficient persulfate activator for the rapid degradation of malachite green, Chemosphere, 2020, 251:126402.
13. Hán Duy Linh, Cao Phương Anh, Cao Việt, Lê Thị Hồng Phong, Nguyễn Xuân Hoàn, Vật liệu composite từ tính Fe3O4/hydroxyapatite ứng dụng trong hấp phụ xử lý 2,4-D và Chrysoidine, VNU Journal of Science, 2021, 37(1):35-43.
14. Mansooreh Dehghani, Simin Nasseri and Mojtaba Karamimanesh, Removal of 2,4-Dichlorophenolyxacetic acid (2,4-D) herbicide in the aqueous phase using modified granular activated carbon, Journal of Environmental Health Science and Engineering, 2014.
15. Ramesh Vinayagam, Saivedh Ganga, Gokulakrishnan Murugesan, Ruchi Bhole, Louella Concepta Goveas, Thivaharan Varadavenkatesan, Niyam Dave, Adithya Samanth, Radhika Devi Raja Selvaraj, 2,4-Dichlorophenoxyacetic acid (2,4-D) adsorptive removal by algal magnetic activated carbon nanocomposite, Chemosphere, 2023, 310:136883.