NGHIÊN CỨU ĐỘC TÍNH CẤP VÀ ĐỘC TÍNH BÁN TRƯỜNG DIỄN CỦA VIÊN NANG CỨNG ĐỊNH THỐNG PHONG TRÊN ĐỘNG VẬT THỰC NGHIỆM
Viện Y sinh Nhiệt đới, Trung tâm Nhiệt đới Việt - Nga
Số 63 Nguyễn Văn Huyên, Nghĩa Đô, Cầu Giấy, Hà Nội
Số điện thoại: 0932215286; Email: tranthanhtuan010182@gmail.com
Nội dung chính của bài viết
Tóm tắt (Abstract)
STUDYING ACUTE AND SUB-CHRONIC TOXICITY OF DINH THONG PHONG CAPSULE IN EXPERIMENTAL ANIMALS
Research to evaluate acute toxicity and sub-chronic toxicity of Dinh Thong Phong capsule (DTP) in experimental animals. Acute toxicity was evaluated in mice follow the method described by Litchfield- Wilcoxon, the OECD guideline and the guideline of Ministry of Health of Vietnam; sub-chronic toxicity was evaluated in rats according to OECD 407 Guideline. In acute toxicity study, no death or toxic signs were observed with DTP capsule administration, DTP capsule did not exhibit acute toxicity up to a dose of 4800 mg/kg. In sub-chronic toxicity, DTP capsule at doses of 500 mg/kg and 1500 mg/kg were had not affect to the body weight; some hematological parameters; AST, ALT, albumin, total cholesterol and creatinine levels; and macroscopic, microscopic images of liver, spleen and kidney of rats when taken continuously for 56 days.
Từ khóa (Keywords)
Acute toxicity, sub-chronic acute toxicity, Dinh Thong Phong capsule, Độc tính cấp, Độc tính bán trường diễn, Viên nang cứng Định Thống Phong
Chi tiết bài viết
1. ĐẶT VẤN ĐỀ
Gút là một loại viêm khớp do sự lắng đọng tinh thể acid uric ở khớp và thường có mối liên quan với tình trạng tăng acid uric huyết [1]. Các thuốc điều trị gút hiện nay gồm thuốc ức chế enzym xanthin oxydase, giúp giảm sản xuất acid uric hoặc thuốc tiêu acid uric (enzym uricase). Các nhóm thuốc này có thể gây tác dụng phụ như dị ứng, phát ban, hội chứng Steven Johnson, đau khớp, nhược cơ, suy giảm chức năng gan, thận. Do đó, thuốc phòng và điều trị bệnh gút từ dược liệu ngày càng được quan tâm, phát triển nhờ ưu điểm có thể dùng lâu dài với tính an toàn cao.
Viên nang cứng Định Thống Phong (ĐTP) là chế phẩm được bào chế từ bài thuốc y học cổ truyền HPA có tác dụng hỗ trợ điều trị bệnh gút trên lâm sàng (gồm các dược liệu: Ngưu tất, tỳ giải, thổ phục linh, hoàng kỳ, ích mẫu, thương truật, thiên niên kiện, trần bì, phá cố chỉ, kê huyết đằng, hà thủ ô đỏ, bán hạ chế, hoạt thạch) bổ sung thêm các vị thuốc dây gắm, hy thiêm thảo, natri bicacrbonat. Theo quy định [2], chế phẩm phải trải qua các giai đoạn thử nghiệm trước khi có thể được sử dụng trên người, trong đó thử nghiệm về độc tính là thử nghiệm đầu tiên. Nghiên cứu này được thực hiện nhằm đánh giá độc tính cấp tính và độc tính bán trường diễn của viên nang cứng ĐTP trên động vật thực nghiệm nhằm cung cấp cơ sở khoa học cho việc sử dụng chế phẩm này trên lâm sàng trong phòng và/hoặc điều trị bệnh gút.
2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Đối tượng nghiên cứu
Viên nang cứng ĐTP đạt tiêu chuẩn cơ sở TCQS 74:2023/NĐVN là sản phẩm của đề tài: “Nghiên cứu bào chế viên nang cứng Định Thống Phong có tác dụng hỗ trợ điều trị bệnh gút trên lâm sàng”/ Trung tâm Nhiệt đới Việt - Nga. Mỗi viên nang có khối lượng 600 mg, chứa 530 mg hỗn hợp bột cao khô ĐTP và natri hydrocarbonat. Công thức bào chế cho 01 viên nang cứng ĐTP như sau:
Bảng 1. Công thức bào chế viên nang cứng ĐTP
Thành phần | Khối lượng |
Hỗn hợp bột cao khô ĐTP và natri hydrocarbonat | 530 mg |
Tá dược (Lactose, avicel, magnesi stearat…) | Vừa đủ 01 viên |
2.2. Động vật thí nghiệm
- Chuột nhắt trắng chủng Swiss, trọng lượng 20 ± 2 g, cả 2 giống, khỏe mạnh do Viện Vệ sinh dịch tễ Trung ương cung cấp.
- Chuột cống trắng chủng Wistar, cả 2 giống, khoẻ mạnh, trọng lượng 180 ± 20 g do Trung tâm Cung cấp động vật thí nghiệm Đan Phượng - Hà Nội cung cấp.
- Động vật được nuôi dưỡng theo chế độ tiêu chuẩn tại phòng thí nghiệm Viện Kiểm nghiệm nghiên cứu dược và trang thiết bị y tế Quân đội từ 5- 7 ngày trước nghiên cứu và trong suốt thời gian nghiên cứu được ăn bằng thức ăn tiêu chuẩn dành riêng, uống nước sạch tự do.
2.3. Máy móc, trang thiết bị, dụng cụ
- Máy xét nghiệm huyết học tự động Coulter LH 780;
- Máy xét nghiệm sinh hóa tự động AU 5800 của hãng Beckman Coulter;
- Bơm tiêm 1 ml và 5 ml; kim uống thuốc đầu tù; dao mổ, kẹp kocher, chày cối, cốc có mỏ, găng tay cao su, khẩu trang y tế…
- Ống xét nghiệm huyết học, sinh hóa, đầu côn các loại.
- Hoá chất xét nghiệm sinh hóa: ALT, AST, cholesterol, albumin, creatinin: Hãng Erba Lachema s.r.o- Czech Republic. Hóa chất xét nghiệm huyết học của hãng B&E Bio-technology Co., Ltd- Trung Quốc.
2.4. Phương pháp nghiên cứu
2.4.1. Độc tính cấp tính
Đánh giá độc tính cấp tính của chế phẩm trên chuột nhắt trắng, theo phương pháp của Litchfield- Wilcoxon [3], hướng dẫn của OECD [4] và của Bộ Y tế Việt Nam [2].
Chuột nhắt trắng cả 2 giống được chia ngẫu nhiên thành 6 lô, mỗi lô 10 con. Chuột được nhịn ăn 12 giờ trước khi thí nghiệm. Cho chuột uống chế phẩm với liều tăng dần với cùng một thể tích (0,2 ml/10g thể trọng) từ liều cao nhất không gây chết tới liều cao nhất có thể cho chuột uống (có thể phân tán được trong nước và chuột có thể uống được). Theo dõi tình trạng chung và số lượng chuột chết ở mỗi lô sau 24 giờ và sau 72 giờ để xác định LD50 (nếu có). Tiếp tục theo dõi tình trạng chung của chuột đến hết ngày thứ 7 sau khi uống.
2.4.2. Độc tính bán trường diễn
Đánh giá độc tính bán trường diễn của chế phẩm được thực hiện theo hướng dẫn của Bộ Y tế [2]. Chuột cống trắng đạt yêu cầu thí nghiệm được chia ngẫu nhiên vào 3 lô, mỗi lô 10 con, uống thuốc cụ thể như sau:
- Lô 1 (lô chứng): Uống nước cất với lượng 4 ml/kg/ngày.
- Lô 2 (lô liều 1): Uống viên nang cứng ĐTP liều 500 mg/kg/ngày.
- Lô 3 (lô liều 2): Uống viên nang cứng ĐTP liều 1500 mg/kg/ngày.
Liều dùng dự kiến của viên nang cứng ĐTP trên người (cân nặng trung bình 50kg) là 6 viên/ngày, tương đương với 72 mg/kg/ngày, nên liều thử độc tính bán trường diễn (hệ số quy đổi liều từ người sang chuột cống trắng là 7) được xác định là 500 mg/kg (tương đương với liều dùng trên người) và 1500 mg/kg (gấp 3 lần liều dùng trên người).
Chuột được cho uống nước cất (lô chứng) hoặc viên nang cứng ĐTP 01 lần/ngày vào buổi sáng liên tục trong 56 ngày.
Chỉ tiêu đánh giá:
- Tình trạng chung, trọng lượng của chuột, các dấu hiệu ngộ độc, tỷ lệ chuột chết được theo dõi trong suốt thời gian nghiên cứu.
- Các mẫu máu được lấy vào các thời điểm: Trước khi uống thuốc, sau khi uống thuốc 28 ngày và 56 ngày ở tất cả các lô nghiên cứu. Các mẫu máu được phân tích các chỉ số huyết học (số lượng hồng cầu - RBC, hemoglobin - HBG, hematocrit - HCT, số lượng bạch cầu - WBC và số lượng tiểu cầu - PLT) và các chỉ số sinh hóa (alanin aminotransferase - ALT, aspartat transaminase - AST, cholesterol toàn phần, albumin và creatinin).
- Sau khi lấy máu vào ngày 56, giết chuột để đánh giá đại thể các cơ quan: gan, lách, thận. Kiểm tra ngẫu nhiên cấu trúc vi thể gan, lách, thận của ít nhất 30% số chuột ở mỗi lô.
2.5. Xử lý số liệu
Các kết quả được trình bày dưới dạng giá trị trung bình ± SD. So sánh sự khác nhau về giá trị trung bình giữa các lô sử dụng phân tích phương sai 1 chiều (One-way ANOVA) và Post Hoc least significant differences (LSD) test với trường hợp phương sai đồng nhất; One-way ANOVA và Dunnett’s T3 test với trường hợp phương sai không đồng nhất. So sánh sự khác biệt về giá trị trung bình giữa các thời điểm trong cùng một lô sử dụng phép so sánh theo cặp (Paired sample T test). Các kết quả thống kê được tính toán trên phần mềm IBM SPSS Statistics 20.0. Sự khác biệt có ý nghĩa thống kê khi p ≤ 0,05.
3. KẾT QUẢ VÀ BÀN LUẬN
3.1. Độc tính cấp tính
Kết quả xác định độc tính cấp tính của viên nang cứng ĐTP được thể hiện trong Bảng 2.
Bảng 2. Độc tính cấp tính theo đường uống của viên nang cứng ĐTP
Lô chuột | Số lượng chuột | Liều sử dụng (mg/kg/ngày) | Số chuột sống/chết | |
Sau 24 giờ | Sau 72 giờ | |||
Lô 1 | 10 | 1638 | 10/0 | 10/0 |
Lô 2 | 10 | 2048 | 10/0 | 10/0 |
Lô 3 | 10 | 2560 | 10/0 | 10/0 |
Lô 4 | 10 | 3200 | 10/0 | 10/0 |
Lô 5 | 10 | 4000 | 10/0 | 10/0 |
Lô 6 | 10 | 4800 | 10/0 | 10/0 |
Qua Bảng 2 cho thấy với các mức liều khác nhau từ 1638 mg/kg/ngày đến 4800 mg/kg/ngày (4800 mg là liều tối đa có thể cho chuột uống, hệ số quy đổi liều từ người sang chuột nhắt trắng là 12), tại tất cả các lô không có chuột nào chết sau 24 giờ và 72 giờ uống thuốc. Ngoài ra, khi theo dõi đến 7 ngày, chuột ở các lô đều khỏe mạnh, không xuất hiện các triệu chứng bất thường hoặc dấu hiệu ngộ độc nào.
Nghiên cứu về độc tính cấp tính là nghiên cứu dược lý đầu tiên cần phải được tiến hành nhằm xác định độc tính xảy ra sau khi dùng thuốc một lần duy nhất hoặc có thể vài ba lần trong ngày [5]. Với các mức liều đã sử dụng ở trên cho thấy viên nang cứng ĐTP chưa xuất hiện độc tính cấp tính.
3.2. Độc tính bán trường diễn
Độc tính bán trường diễn được tiến hành sau khi có dữ liệu về độc tính cấp tính của chế phẩm; Nghiên cứu độc tính bán trường diễn nhằm đánh giá khả năng dung nạp của động vật khi tiếp xúc nhiều lần với thuốc. Trong thời gian dùng thuốc có ảnh hưởng đáng kể nào đến chức năng hoặc cơ quan không? Những độc tính có thể quan sát được là gì? Và khả năng hồi phục ra sao? [2]. Thời gian thử nghiệm lựa chọn trong nghiên cứu là 56 ngày.
3.2.1. Ảnh hưởng tới thể trạng chung, dấu hiệu ngộ độc và trọng lượng cơ thể chuột
Trong suốt thời gian nghiên cứu, thể trạng chung của chuột bình thường, không thấy bất kỳ chuột nào có dấu hiệu ngộ độc hoặc chết ở tất cả các lô; chuột ăn, uống bình thường, mắt trong, lông mượt, phân khô.
Trọng lượng cơ thể chuột được trình bày trong Bảng 3.
Bảng 3. Trọng lượng cơ thể chuột (g) ở các lô theo thời gian (n = 10)
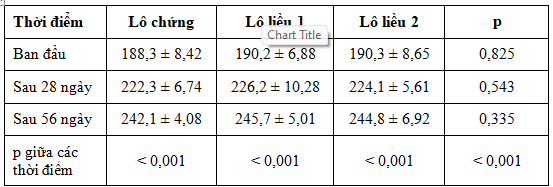
Qua kết quả trên cho thấy, không có sự khác biệt có ý nghĩa (p > 0,05) về trọng lượng cơ thể chuột giữa các lô ở cùng thời điểm nghiên cứu.
3.2.2. Ảnh hưởng tới một số chỉ số huyết học
* Một số chỉ số về hồng cầu:
Ảnh hưởng của viên nang cứng ĐTP tới số lượng hồng cầu, hemoglobin, hematocrit máu chuột được trình bày trong Bảng 4.
Bảng 4. Ảnh hưởng của viên nang cứng ĐTP lên RBC, HBG và HCT (n = 10)
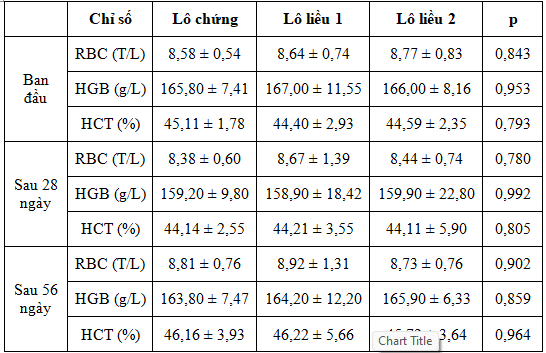
Kết quả trên cho thấy không có sự khác biệt có ý nghĩa về RBC, HGB và HCT giữa các lô ở cùng một thời điểm nghiên cứu (p > 0,05); đồng thời không có sự khác biệt có ý nghĩa (p > 0,05) về RBC, HGB và HCT giữa các thời điểm trong cùng một lô.
Sự sản xuất hồng cầu được điều hòa bởi erythropoietin, một hormon được sản xuất chủ yếu từ thận (80- 90%, phần còn lại ở gan) [6]. Trên người, hồng cầu tăng có thể do một số nguyên nhân như: Hút thuốc, thiếu oxy động mạch mạn tính, khối u (tăng hồng cầu do khối u), sử dụng steroid hướng thượng thận, sử dụng erythropoietin, các bệnh huyết sắc tố có ái lực với oxy cao, các đột biến với thụ thể của erythropoietin, các shunt phải - trái động tĩnh mạch phổi; ngoài ra, tăng hồng cầu giả có thể xảy ra với sự cô đặc máu (do bỏng, tiêu chảy, hoặc sử dụng thuốc lợi tiểu) [7]. Số lượng hồng cầu, HGB và HCT giảm có thể do giảm sản xuất hồng cầu (giảm sinh hồng cầu), tăng phá hủy hồng cầu, mất máu, hoặc phối hợp các yếu tố này. Ở các lô dùng ĐTP không có sự khác biệt có ý nghĩa về RBC, HGB và HCT so với lô chứng và ở các thời điểm sau 28 ngày và 56 ngày không có sự khác biệt có ý nghĩa với thời điểm ban đầu; do đó, viên nang cứng ĐTP liều 500 mg/kg/ngày và 1500 mg/kg/ngày trong 56 ngày không làm ảnh hưởng tới RBC, HGB và HCT.
* Số lượng bạch cầu và số lượng tiểu cầu
Ảnh hưởng của viên nang cứng ĐTP tới số lượng bạch cầu và số lượng tiểu cầu máu chuột được trình bày trong Bảng 5.
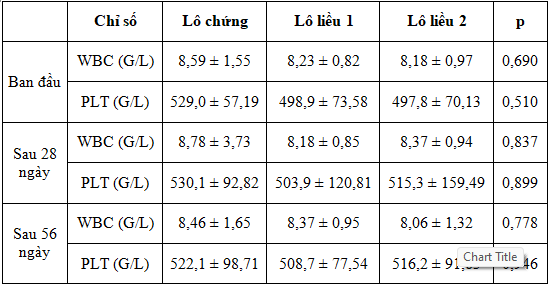
Bảng 5. Ảnh hưởng của viên nang cứng ĐTP lên WBC và PLT (n = 10)
WBC giảm khi tủy xương giảm hoặc ngừng sản xuất bạch cầu [6], điều này có thể xuất phát từ việc dùng thuốc, nhiễm trùng và phản ứng miễn dịch, quá trình thâm nhiễm tủy xương. Trong đó, phổ biến nhất là giảm do thuốc. Thuốc có thể làm giảm quá trình sản sinh bạch cầu thông qua các cơ chế gây độc, đặc ứng hoặc quá mẫn; hoặc chúng có thể làm gia tăng sự phá hủy bạch cầu trung tính ngoại vi thông qua các cơ chế miễn dịch. WBC tăng có nguyên nhân phổ biến nhất là do cơ thể gặp phải tình trạng nhiễm trùng, do bệnh bạch cầu (ung thư máu) ngoài ra còn gặp trong một số bệnh lý tim mạch, bệnh nhân chạy thận nhân tạo [8].
Tiểu cầu giảm có thể do các nguyên nhân: Giảm tiểu cầu giả (là hiện tượng trong đó số lượng tiểu cầu được đếm bởi máy tự động thấp hơn nhiều so với số lượng tiểu cầu thực sự lưu hành trong cơ thể; nguyên nhân do chất chống đông EDTA, do tiểu cầu vệ tinh và do tiểu cầu kích thước lớn) [9]; giảm sự sản xuất của tiểu cầu; tăng phá hủy của tiểu cầu (trong đó có nhiều thuốc làm tăng sự phá hủy của tiểu cầu) hoặc bất thường về sự phân bố của tiểu cầu [10]. Việc giảm tiểu cầu giả thường xảy ra trong thực hành lâm sàng khi việc phân tích tiểu cầu được thực hiện cùng với bạch cầu (bằng máy tự động) [9].
Kết quả từ Bảng 5 cho thấy không có sự khác biệt có ý nghĩa về WBC và PLT giữa các lô ở cùng một thời điểm nghiên cứu (p > 0,05) và giữa các thời điểm khác nhau trong cùng một lô. Như vậy viên nang cứng ĐTP liều 500 mg/kg/ngày và 1500 mg/kg/ngày trong 56 ngày không làm ảnh hưởng tới WBC và PLT.
3.2.3. Ảnh hưởng tới một số chỉ số sinh hóa máu
* Hoạt độ enzym AST và ALT
Ảnh hưởng của viên nang cứng ĐTP tới số hoạt độ enzym AST (U/L) và hoạt độ enzym ALT (U/L) máu chuột được trình bày trong Bảng 6.
Bảng 6. Ảnh hưởng của viên nang cứng ĐTP lên hoạt độ AST và ALT (n = 10)
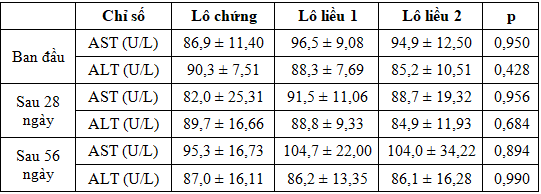
Kết quả cho thấy, khi so sánh giữa các lô: không có sự khác biệt có ý nghĩa thống kê (p > 0,05) về hoạt độ enzym AST và ALT ở cùng một thời điểm nghiên cứu. Khi so sánh giữa các thời điểm khác nhau trong cùng một lô cũng nhận thấy không có sự khác biệt có ý nghĩa (p > 0,05) về hoạt độ enzym AST và ALT.
AST và ALT nói chung là những enzym hữu ích nhất để xác định sự hiện diện của tổn thương tế bào gan. AST và ALT được tìm thấy trong một số mô nhưng chủ yếu và nhiều nhất là ở gan [11]. Sự tăng hoạt độ AST và ALT phần nhiều do sự tổn thương của tế bào gan, sự giảm hoạt độ các enzym này có thể do tác dụng bảo vệ tế bào gan của chế phẩm nghiên cứu. Trong nghiên cứu này, hoạt độ AST và ALT của các lô dùng chế phẩm nghiên cứu khác nhau không có ý nghĩa so với lô chứng. Như vậy uống viên nang cứng ĐTP liều 500 mg/kg/ngày và 1500 mg/kg/ngày trong 56 ngày không làm ảnh hưởng tới chức năng gan chuột.
* Nồng độ cholesterol
Ảnh hưởng của viên nang cứng ĐTP tới số nồng độ cholesterol toàn phần (mmol/L) máu chuột được trình bày trong Hình 1.
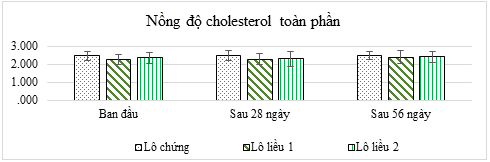
Hình 1. Ảnh hưởng của viên nang cứng ĐTP lên nồng độ cholesterol toàn phần (n = 10)
Không có sự khác biệt có ý nghĩa về nồng độ cholesterol toàn phần máu chuột giữa các lô ở cùng một thời điểm (p > 0,05). Đồng thời, khi so sánh giữa các thời điểm nghiên cứu khác nhau trong cùng một lô cũng nhận thấy không có sự khác biệt có ý nghĩa (p > 0,05) về nồng độ cholesterol toàn phần máu chuột. Như vậy, viên nang cứng ĐTP không làm ảnh hưởng tới nồng độ cholesterol toàn phần máu chuột.
* Nồng độ albumin
Ảnh hưởng của viên nang cứng ĐTP tới số nồng độ albumin (g/L) máu chuột được trình bày trong Hình 2.
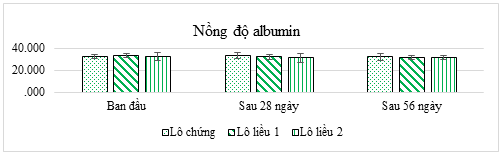
Hình 2. Ảnh hưởng của viên nang cứng ĐTP lên nồng độ albumin (n = 10)
Tại các thời điểm nghiên cứu, không có sự khác nhau về nồng độ albumin trong máu chuột giữa các lô (p > 0,05). Đồng thời, khi so sánh trong cùng một lô cũng không có sự khác biệt về nồng độ albumin giữa các thời điểm nghiên cứu (p > 0,05). Như vậy viên nang cứng ĐTP không làm ảnh hưởng tới nồng độ albumin máu chuột.
* Nồng độ creatinin
Ảnh hưởng của viên nang cứng ĐTP tới số nồng độ creatinin (mmol/L) máu chuột được trình bày trong Hình 3.

Hình 3. Ảnh hưởng của viên nang cứng ĐTP lên nồng độ creatinin (n = 10)
Creatinin là sản phẩm của sự thoái hóa creatin trong các cơ, được đào thải qua thận. Khi chức năng thận bị suy giảm thì khả năng lọc creatinin giảm dẫn tới nồng độ creatinin trong máu sẽ tăng cao hơn bình thường. Nồng độ creatinin thấp thường gặp ở người cao tuổi; suy dinh dưỡng nặng; sụt cân nghiêm trọng hoặc các bệnh mạn tính kéo dài mà khối lượng cơ có xu hướng giảm dần theo thời gian [12]. Kết quả trên cho thấy không có sự khác biệt có ý nghĩa (p > 0,05) về nồng độ creatinin máu chuột giữa các lô tại một thời điểm và giữa các thời điểm trong cùng một lô; do vậy, viên nang cứng ĐTP ở 2 mức liều nghiên cứu không làm ảnh hưởng đến nồng độ creatinin máu chuột.
3.2.4. Hình ảnh đại thể, vi thể một số cơ quan
* Hình ảnh đại thể
Hình ảnh đại thể gan, lách và thận chuột ở các lô được thể hiện trong Hình 4.

Hình 4. Hình ảnh đại thể gan, lách và thận chuột.
Ghi chú: (a): lô chứng; (b): lô liều 1; (c): lô liều 2
Quan sát đại thể bằng mắt thường dưới kính lúp, cho thấy: màu sắc, hình thái của gan, lách và thận ở hai lô dùng viên nang cứng ĐTP (ảnh b và ảnh c) có màu nâu đỏ thẫm đồng đều, bề mặt nhẵn, không có u cục hoặc xuất huyết, có đàn hồi khi ấn xuống. Không có sự khác biệt khi so với hình ảnh gan, lách, thận của chuột ở lô chứng (ảnh a).
* Hình ảnh vi thể
Hình ảnh vi thể gan (Hình 5): Ở các lô đều thấy: các bè gan, tiểu thùy gan và tế bào gan bình thường, không có hình ảnh thoái hóa hoặc viêm, tĩnh mạch trung tâm không giãn, các xoang mạch nan hoa và tĩnh mạch khoảng cửa không xung huyết.
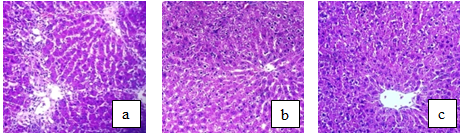
Hình 5. Hình ảnh vi thể gan chuột ở các lô
Ghi chú: Nhuộm HE (400X); (a): lô chứng; (b): lô liều 1; (c): lô liều 2
Hình ảnh vi thể lách (Hình 6): Tại tất cả các lô: lách rõ cấu trúc vùng vở và vùng tủy, vùng vỏ có các nang lympho lớn với động mạch bút lông. Không có xuất huyết, hoại tử.
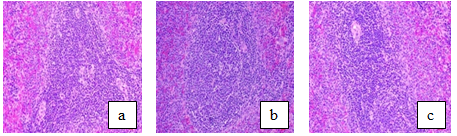
Hình 6. Hình ảnh vi thể lách chuột ở các lô
Ghi chú: Nhuộm HE (400X); (a): lô chứng; (b): lô liều 1; (c): lô liều 2
Hình ảnh vi thể thận (Hình 7): Ở tất cả các lô đều thấy: Các tiểu cầu thận với mao cuộn mạch rõ, các tế bào ống thận bình thường.
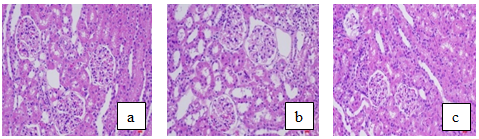
Hình 7. Hình ảnh vi thể thận chuột ở các lô
Ghi chú: Nhuộm HE (400X); (a): lô chứng; (b): lô liều 1; (c): lô liều 2
Như vậy, viên nang cứng ĐTP ở 2 mức liều nghiên cứu không ảnh hưởng tới hình ảnh vi thể gan, lách, thận chuột.
4. KẾT LUẬN
Đã đánh giá được độc tính cấp tính và độc tính bán trường diễn của viên nang cứng ĐTP trên động vật thực nghiệm. Kết quả cho thấy, khi dùng đến liều 4800 mg/kg, viên nang cứng ĐTP không xuất hiện độc tính cấp tính ở các mức liều đã thử nghiệm, chưa xác định được LD50 trên thực nghiệm; với 2 mức liều 500 mg/kg và 1500 mg/kg trên chuột cống trắng trong thời gian 56 ngày đã không làm ảnh hưởng tới trọng lượng cơ thể; các chỉ số huyết học; hoạt độ enzym AST, ALT; nồng độ albumin, cholesterol toàn phần, creatinin; hình ảnh đại thể và vi thể gan, lách, thận chuột.
Tài liệu tham khảo
2. Trương Quốc Cường, Thông tư số 29/2018/TT-BYT: Quy định về Thử thuốc trên lâm sàng, 2018.
3. Litchfield J. T. and Wilcoxon F., A simplified method of evaluating dose-effect experiments, Journal of Pharmacology and Experimental Therapeutics, 1949, 96(2):99-113.
4. OECD, Test No, 420: Acute Oral Toxicity - Fixed Dose Procedure, 2002. doi: 10.1191/0960327102ht239oa.
5. Đỗ Trung Đàm, Phương pháp xác định độc tính của thuốc, Nhà xuất bản Y học, Hà Nội, 2014.
6. Phạm Thị Minh Đức, Trịnh Bỉnh Dy, Lê Thu Liên và cs., Sinh lý học, Nhà xuất bản Y học, Hà Nội, 2011.
7. McMullin M. F., Secondary erythrocytosis, Hematology, 2014, 19(3):183-184. doi: 10.1179/1024533214Z.000000000263.
8. Reddan Donal N., Klassen Preston S., Szczech Lynda A., et al., White blood cells as a novel mortality predictor in haemodialysis patients, Nephrology dialysis transplantation, 2003, 18(6):1167-1173. doi: 10.1093/ndt/gfg066.
9. Zandecki M., Genevieve F., Gerard J., et al., Spurious counts and spurious results on haematology analysers: a review. Part I: platelets, International Journal of Laboratory Hematology, 2007, 29(1):4-20. doi: 10.1111/j.1365-2257.2006.00870.
10. Erkurt Mehmet Ali, Kaya Emin, Berber Ilhami, et al., Thrombocytopenia in adults, Journal of Hematology, 2012, 1(2-3):44-53. doi: https://doi.org/10.4021/jh28w.
11. York Malcolm J., Clinical pathology, In: A comprehensive guide to toxicology in nonclinical drug development, Elsevier,, 2017, p. 325-374, doi: https://doi.org/10.1016/B978-0-12-803620-4.00014-1.
12. Diago Carlos A Amado and Señaris José A Amado, Should we pay more attention to low creatinine levels?, Endocrinología, Diabetes y Nutrición (English ed.), 2020, 67(7):486-492, doi: 10.1016/j.endinu.2019.12.008.