XÁC ĐỊNH ACETAMIPRID BẰNG PHƯƠNG PHÁP QUANG HỌC SỬ DỤNG DUNG DỊCH NANO VÀNG ĐƯỢC ỔN ĐỊNH BẰNG POLYDIALLYLDIMETHYLAMMONI CLORUA
Viện Độ bền Nhiệt đới, Trung tâm Nhiệt đới Việt - Nga
Số 63 Nguyễn Văn Huyên, Nghĩa Đô, Cầu Giấy, Hà Nội
Số điện thoại: 0358945500; Email: lethithaohus@gmail.com
Nội dung chính của bài viết
Tóm tắt (Abstract)
DETERMINATION OF ACETAMIPRID BY SPECTROPHOTOMETRIC METHOD USING GOLD NANOPARTICLES STABILIZED WITH POLYDIALLYLDIMETHYLAMMONIUM CHLORIDE
On this research, the development of a simple, cost-efective and highly sensitive spectrophotometric method for acetamiprid detection based on the localized surface plasmon resonance of polydiallyldimethylammonium chloride-stabilized gold nanoparticles. By naked eyes, one can detect acetamiprid by the visual change of gold solution color from red to purple, corresponding to the shift of maximum absorbance wavelength in the UV-Vis spectrum. Quantification of acetamiprid is possible through a linear relationship between the maximum absorbance wavelength and the acetamiprid concentrations in the range of 8×10-8 - 2×10-6 M. Under the optimum conditions including pH 5, NaCl concentration of 0.02 M and incubation time 20 min, the present method has high precision (RSD < 5%), very low limit of detection (LOD) of 2.7×10-8 M, limit of quantification (LOQ) of 8.2×10-8 M. This method has been successfully applied to determine acetamiprid in several pesticide samples and vegetable samples. The measurement results of acetamiprid in the pesticide samples of the research method with the HPLC-UV method showed a difference of < 2%, while for the vegetable sample, the difference between the research method and the LC-MS/method method/ MS < 5% shows that the method has high accuracy and reliability.
Từ khóa (Keywords)
Acetamiprid determination, UV-Vis absorption, gold nanoparticles, PDADMAC, hạt nano vàng AuNPs.
Chi tiết bài viết
1. ĐẶT VẤN ĐỀ
Acetamiprid (C10H11ClN4) là hoạt chất thuộc nhóm neonicotinoid không mùi, có tác dụng phòng trừ và kiểm soát các loại côn trùng trích hút trên các loại cây trồng như rau, hoa quả, cây cảnh, nên được dùng phổ biến trong nông nghiệp [1, 2]. Tuy nhiên, dư lượng tồn đọng của acetamiprid trong nhiều loại cây trồng, trái cây có thể gây ra nhiều tác động xấu đến sức khỏe con người. Acetamiprid chủ yếu tác động đến hệ thần kinh trung ương gây chóng mặt, nhức đầu, nặng hơn có thể bị kích động, co giật và hôn mê [1, 2]. Vì vậy, việc xác định dư lượng acetamiprid là rất cần thiết để bảo vệ sức khỏe con người.
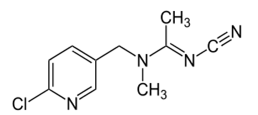
Hình 1. Cấu trúc phân tử của acetamiprid
Hiện nay, nhiều nghiên cứu khoa học tập trung hướng tới các phương pháp xác định hàm lượng acetamiprid một cách nhanh, nhạy và chính xác nhất. Có nhiều phương pháp được sử dụng để xác định hàm lượng acetamiprid như phương pháp sắc ký lỏng hiệu năng cao (HPLC) [3], sắc ký lỏng ghép nối khối phổ (LC/MS) [4], sắc ký khí ghép nối khối phổ (GC/MS) [5], điện hóa [6], phương pháp phổ huỳnh quang [7]. Tuy nhiên, các phương pháp này có một số nhược điểm như thiết bị đắt tiền, vận hành phức tạp, đòi hỏi phải xử lý mẫu.
Mục tiêu của nghiên cứu này là phát triển một phương pháp phân tích xác định hàm lượng acetamiprid với quy trình đơn giản, không tốn kém về hóa chất và trang thiết bị nhưng có độ nhạy và độ chính xác cao. Vật liệu nano vàng (AuNPs) ngày càng được quan tâm rộng rãi bởi các đặc tính độc đáo của chúng, đặc biệt là hiện tượng cộng hưởng plasmon bề mặt. Gần đây, tại Việt Nam các phương pháp quang học sử dụng dung dịch AuNPs đã được ứng dụng để xác định các kháng sinh [8, 9], chất bảo vệ thực vật [10], cystein [11],… Tuy nhiên chưa có nghiên cứu nào sử dụng dung dịch AuNPs ổn định bằng polyme điện tích dương polydiallyldimethylammoni clorua (PDADMAC) để xác định thuốc trừ sâu acetamiprid. Vì vậy, mục tiêu của bài báo này là nghiên cứu sử dụng hiện tượng plasmon bề mặt của dung dịch nano vàng được ổn định bằng PDADMAC với khả năng làm thay đổi màu sắc dung dịch từ đỏ sang tím khi có mặt acetamiprid để phát hiện sự có mặt và định lượng acetamiprid trong các mẫu thuốc trừ sâu và rau củ quả.
2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Hóa chất, thiết bị
Các hóa chất được sử dụng là các hóa chất tinh khiết phân tích (PA): Chloroauric acid tetrahydrat (HAuCl4.4H2O), polydiallyldimethylammoni clorua (PDADMAC), natri bohidrua (NaBH4), natri clorua (NaCl), natri hydroxit (NaOH), hydrochloric acid (HCl), chất chuẩn các thuốc bảo vệ thực vật (acetamiprid, methidathion, ethion, dichlorvos, phorate, carbendazim, aldicarb, carbaryl). Thuốc bảo vệ thực vật chứa acetamiprid: KHONGRAY 54WP, Chesone 300WP, Ba Đăng 500WP.
Máy đo pH HI2210-02 -HANNA (Romania), thang đo pH từ -2 đến 16. Máy quang phổ hấp thụ phân tử UV-VIS DR6000-HACH (Mỹ), bước sóng làm việc từ 400-800 nm.
2.2. Điều chế dung dịch nano vàng
Lấy 20 mL PDADMAC 0,008 ppm và 500 µL HAuCl4.3H2O 10 mM vào cốc chịu nhiệt 100 ml. Khuấy mạnh bằng thiết bị khuấy từ trong khoảng 5 phút. Thêm 600 μL NaBH4 0,05M, tiếp tục khuấy dung dịch trong khoảng 15 phút đến khi dung dịch chuyển sang màu đỏ rượu biểu thị sự hình thành các hạt AuNPs. Dung dịch sau đó được làm mát đến nhiệt độ phòng và bảo quản ở 4°C trong tủ lạnh.
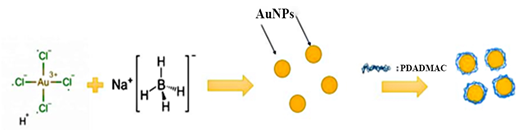
Hình 2. Sơ đồ sự hình thành các hạt AuNPs-PDADMAC
2.3. Nguyên tắc định lượng acetamiprid
Các hạt AuNPs được điều chế bằng phương pháp sử dụng PDADMAC có điện tích dương do có sự bao phủ của các cation trên bề mặt. Lớp điện kép mang điện tích dương trên bề mặt hạt nano vàng có tác dụng đẩy các hạt AuNPs ra khỏi nhau giúp các hạt AuNPs được ổn định. Dung dịch AuNPs-PDADMAC có màu đỏ rượu với cực đại hấp thụ đặc trưng tại bước sóng λmax = 519 nm, kích thước hạt cỡ 20 nm (Hình 3).
Khi acetamiprid có mặt trong dung dịch AuNPs-PDADMAC, acetamiprid có khả năng hấp phụ rất tốt trên các hạt AuNPs do trong phân tử có chứa nhóm -NH có ái lực cao với vàng. Khi đó, các hạt PDADMAC-AuNPs kết tụ lại với nhau thông qua tương tác kị nước giữa các phân tử acetamiprid (Hình 4) và làm cho dung dịch chuyển từ màu đỏ rượu sang màu tím. Đồng thời, bước sóng hấp thụ cực đại của dung dịch có chất phân tích acetamiprid cũng tăng lên đáng kể so với dung dịch không có acetamiprid [11].
Thiết lập mối quan hệ giữa sự gia tăng bước sóng cực đại hấp thụ với nồng độ của acetamiprid có trong dung dịch AuNPs-PDADMAC để làm cơ sở định lượng acetamiprid.

Hình 3. Hình thái của các hạt nano vàng khi được ổn định bằng PDADMAC (trái) và khi có mặt acetamiprid (phải)
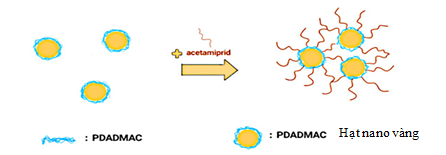
Hình 4. Cơ chế xác định acetamiprid với các hạt AuNPs-PDADMAC
2.4. Xử lý mẫu phân tích
Nghiên cứu trên 3 mẫu thuốc trừ sâu có chứa acetamiprid (KHONGRAY 54WP chứa 24% acetamiprid, Chesone 300WP chứa 10% acetamiprid, Ba Đăng 500WP chứa 15% acetamiprid) và 3 mẫu rau, củ không phát hiện thấy acetamiprid (rau cải, dưa chuột, cà chua) được mua ngẫu nhiên trên thị trường tại tỉnh Hải Dương và Hà Nội được thêm chuẩn acetamiprid.
Mẫu thuốc trừ sâu KHONGRAY 54WP được cân chính xác 0,0464 g trên cân phân tích (sai số 0,0001 g), hòa tan bằng nước cất và rung siêu âm đến khi chất phân tích tan hết. Chuyển mẫu thuốc vào bình định mức 50 mL, định mức đến vạch bằng nước deion, sau đó pha loãng 10 lần thu được dung dịch mẫu 1. Chuẩn bị bình định mức dung tích 10 mL, cho vào 4,0 mL dung dịch AuNPs-PDADMAC, thêm 200 µL dung dịch NaCl 1M, chỉnh pH 5, thêm 30 µL dung dịch mẫu 1 và định mức đến vạch. Đợi 20 phút và xác định giá trị bước sóng hấp thụ cực đại λmax. Hàm lượng acetamiprid trong mẫu thuốc trừ sâu được xác định bằng phương pháp đường chuẩn.
Tiến hành quy trình tương tự với mẫu thuốc trừ sâu Chesone 300 WP và mẫu thuốc trừ sâu Ba Đăng 500 WP với lượng cân chính xác của mẫu Chesone 300WP và mẫu Ba Đăng lần lượt là 0,1113 g và 0,0742 g.
Mẫu rau cải, dưa chuột và cà chua: Cân chính xác 5 g mẫu, xay mịn, thêm 50 µL dung dịch chuẩn acetamiprid nồng độ 5×10-3 M. Thêm 10 mL acetonitril, ủ trong 30 phút. Sau đó, tiến hành ly tâm lạnh (7°C) ở 10.000 vòng/phút trong 15 phút (quy trình ủ và ly tâm được lặp lại 2 lần). Thu lấy phần dung dịch phía trên, thêm 1 g than hoạt tính, tiếp tục ly tâm lạnh (7°C) ở 10.000 vòng/phút trong 15 phút. Hút lấy phần dung dịch trong suốt phía trên và làm bay hơi bằng khí N2. Phần cặn thu được sau đó được hòa tan với 2 mL acetonitril, thu được dung dịch mẫu A. Chuẩn bị bình định mức dung tích 10 ml, cho vào bình 4,0 mL dung dịch AuNPs-PDADMAC, thêm 200 µL dung dịch NaCl 1M, chỉnh pH 5, thêm 40 µL dung dịch mẫu A, định mức đến vạch. Đợi 20 phút và xác định giá trị λmax.
3. KẾT QUẢ VÀ THẢO LUẬN
3.1. Tối ưu hóa các điều kiện đo xác định hàm lượng acetamiprid
3.1.1. Phổ hấp thụ quang và khảo sát bước sóng hấp thụ cực đại (λmax) của dung dịch AuNPs-PDADMAC
Hình 5 cho thấy phổ hấp thụ quang UV-VIS của dung dịch AuNPs-PDADMAC có đỉnh hấp thụ cực đại tại bước sóng 519 nm (dải hấp thụ cộng hưởng plasmon bề mặt). Sau khi cho thêm acetamiprid nồng độ 10-6 M, đỉnh hấp thụ quang cực đại đã tăng lên 622 nm. Nguyên nhân là do sự thay đổi kích thước hạt nano vàng khi có mặt acetamiprid dẫn đến sự dịch chuyển cực đại hấp thụ từ bước sóng 519 nm sang 622 nm đồng thời với sự thay đổi màu sắc của dung dịch AuNPs-PDADMAC từ đỏ sang tím [11].
Từ khảo sát trên, chúng tôi lựa chọn sự thay đổi của bước sóng hấp thụ quang cực đại làm tín hiệu phân tích để định lượng acetamiprid.
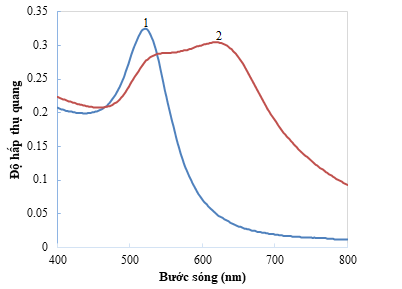
Hình 5. Phổ hấp thụ của dung dịch AuNPs-PDADMAC khi chưa có mặt của acetamiprid (đường 1) và khi có mặt của acetamiprid (nồng độ 10-6 M) (đường 2)
3.1.2. Ảnh hưởng của nồng độ muối NaCl đến λmax
Ảnh hưởng của chất điện ly được xem như là khởi đầu cho sự co cụm của các hạt nano vàng do chúng tạo ra lớp điện kép trên bề mặt các hạt nano vàng. Trong một số trường hợp, các hạt nano vàng không thể co cụm lại khi không có chất điện ly ngay cả khi có mặt một lượng lớn chất phân tích. Ngoài ra, nếu chất điện ly có nồng độ quá cao sẽ gây ra hiện tượng co cụm các hạt nano vàng kể cả khi không có mặt chất phân tích [11]. Kết quả nghiên cứu khảo sát ảnh hưởng của muối NaCl với nồng độ từ 0,005 M đến 0,05 M đến bước sóng cực đại của dung dịch AuNPs- PDADMAC chứa acetamiprid nồng độ 8×10-7 M tại pH 5 và thời gian phản ứng 15 phút, được thể hiện trong Hình 6.
Khi tăng nồng độ muối NaCl từ 0,005 M đến 0,05 M, bước sóng cực đại có xu hướng tăng cho thấy khả năng co cụm của các hạt nano vàng tăng khi tăng cường độ lực ion của dung dịch và đạt bão hòa khi nồng độ NaCl tại 0,03 M và sau đó giảm nhẹ. Tuy nhiên, tại nồng độ 0,03M, dung dịch AuNPs- PDADMAC bắt đầu bị đổi màu rõ rệt ngay cả khi chưa có chất phân tích, gây ảnh hưởng đến quá trình quan sát sự thay đổi của dung dịch khi thêm chất phân tích. Do đó, nồng độ 0,02 M được chọn là điều kiện tối ưu cho các thí nghiệm tiếp theo.
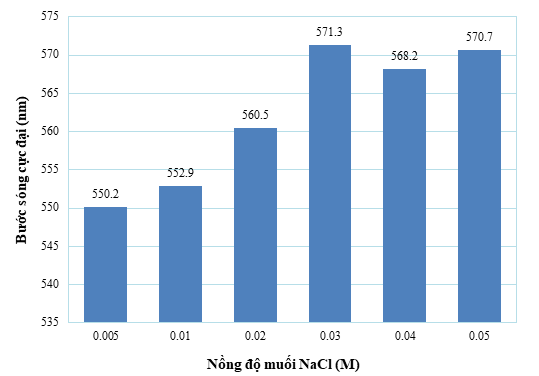
Hình 6. Ảnh hưởng của NaCl đến bước sóng cực đại λmax
3.1.3. Ảnh hưởng của pH đến λmax
Trên Hình 7 là kết quả nghiên cứu khảo sát ảnh hưởng của pH trong khoảng từ 4 đến 9 lên bước sóng cực đại của dung dịch AuNPs-PDADMAC chứa acetamiprid nồng độ 8×10-7 M, nồng độ NaCl là 0,02 M, thời gian phản ứng 15 phút.
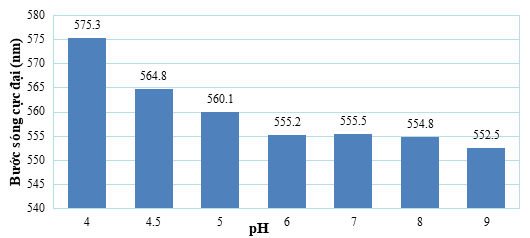
Hình 7. Ảnh hưởng của pH đến bước sóng cực đại λmax
Tại pH 4 bước sóng cực đại là lớn nhất, sau đó giảm mạnh khi tăng pH đến 9. Tuy nhiên, tại pH 4 và 4,5 dung dịch AuNPs-PDADMAC bắt đầu bị đổi màu rõ rệt ngay cả khi chưa có chất phân tích, do đó, pH 5 được chọn là điều kiện tối ưu cho các thí nghiệm tiếp theo.
3.1.4. Ảnh hưởng của thời gian phản ứng đến λmax
Thời gian phản ứng là một yếu tố quan trọng trong việc xác định mức độ co cụm của các hạt nano vàng. Khảo sát ảnh hưởng của thời gian bằng cách ghi lại bước sóng cực đại của dung dịch AuNPs-PDADMAC chứa acetamiprid nồng độ 8×10-7 M, nồng độ NaCl 0,02 M, pH 5, trong thời gian 40 phút, kết quả được thể hiện trong Hình 8.
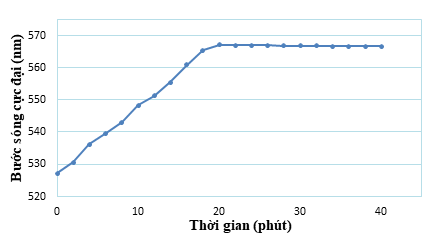
Hình 8. Ảnh hưởng của thời gian đến bước sóng cực đại λmax
Kết quả thực nghiệm cho thấy bước sóng cực đại tăng dần trong 20 phút đầu, sau đó ổn định và không đổi, cho thấy hiện tượng co cụm của các hạt nano vàng bắt đầu xảy ra ngay sau khi có mặt acetamiprid và kết thúc sau 20 phút. Sau khi thêm acetamiprid, dung dịch chuyển từ màu đỏ rượu sang tím (tương ứng với sự co cụm của các hạt nano vàng) và màu bền vững sau 20 phút. Do đó, thời gian phản ứng 20 phút được lựa chọn là điều kiện tối ưu cho phương pháp xác định acetamiprid.
3.1.5. Ảnh hưởng của nồng độ acetamiprid đến λmax
Nồng độ acetamiprid được khảo sát trong khoảng nồng độ từ 10-7 M - 2×10-6 M tại nồng độ NaCl 0,02M, pH 5, thời gian phản ứng 20 phút. Ghi các phổ UV-VIS trong khoảng bước sóng từ 400 đến 800 nm, kết quả được thể hiện trên Hình 9.
Khi tăng nồng độ acetamiprid, có sự dịch chuyển bước sóng cực đại sang bước sóng dài hơn (red-shift). Khi xây dựng mối quan hệ giữa bước sóng cực đại và nồng độ acetamiprid thu được mối quan hệ tuyến tính trong khoảng nồng độ khảo sát. Đây cũng chính là cơ sở để định lượng acetamiprid bằng dung dịch AuNPs-PDADMAC.
Từ những khảo sát trên, nghiên cứu lựa chọn được các điều kiện đo tối ưu như sau: pH 5, nồng độ muối NaCl 0,02 M, thời gian phản ứng 20 phút cho các phân tích xác định hàm lượng acetamiprid trong các mẫu thực tế.
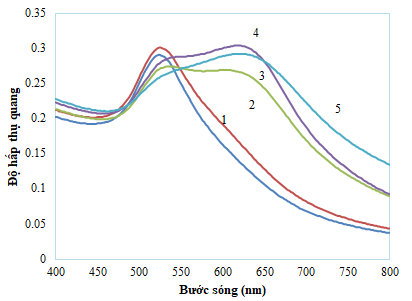
Hình 9. Phổ hấp thụ quang của dung dịch AuNPs-PDADMAC với các nồng độ acetamiprid khác nhau (Đường từ 1 đến 5 tương ứng là 10-7 M, 2×10-7 M, 4×10-7 M, 6×10-7 M, 2×10-6 M)
3.2. Đánh giá phương pháp
Đánh giá phương pháp thông qua khảo sát khoảng tuyến tính, dựng đường chuẩn, xác định giới hạn phát hiện (LOD), giới hạn định lượng (LOQ), độ đúng, độ lặp lại.
Tiến hành đo các dung dịch acetamiprid có nồng độ khác nhau từ 8×10-8 - 6×10-6 M tại điều kiện tối ưu (CNaCl= 0,02 M, pH 5, thời gian phản ứng 20 phút).
Kết quả cho thấy bước sóng cực đại tuyến tính theo nồng độ của acetamiprid trong khoảng từ 8×10-8 - 2×10-6 M. Đường chuẩn xây dựng trong khoảng nồng độ này có phương trình: λmax = 6×107 ×Cacetamiprid + 517 với hệ số tương quan cao R2=0,9992.
LOD, LOQ được xác định từ phương trình đường chuẩn theo công thức LOD = 3Sy/b và LOQ = 10Sy/b với Sy là độ lệch chuẩn của mẫu trắng và b là hệ số góc của phương trình đường chuẩn. Kết quả thu được giá trị LOD là 2,7×10-8 M và LOQ là 8,2×10-8 M.
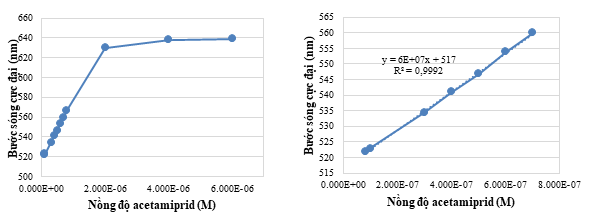
Hình 10. Đồ thị khảo sát khoảng tuyến tính Hình 11. Đồ thị xây dựng đường chuẩn
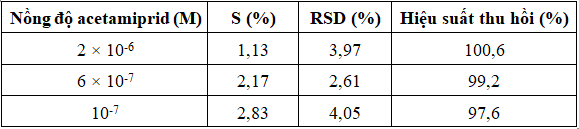
Độ đúng và độ lặp lại của phương pháp được đánh giá thông qua sai số trung bình (S%), độ lệch chuẩn tương đối (% RSD), hiệu suất thu hồi (%) khi tiến hành đo lặp lại 10 lần các dung dịch AuNPs-PDADMAC chứa acetamiprid ở 3 mức nồng độ là 2×10-6 M, 6×10-7 M và 10-7 M. Kết quả đo được (Bảng 1) cho thấy giá trị độ lệch chuẩn tương đối (RSD) đều dưới 5% đáp ứng yêu cầu AOAC (Association of Official Analytical Chemists - Hiệp hội các nhà hóa học phân tích chính thống) và hiệu suất thu hồi đạt từ 97,6% đến 100,6%:
Bảng 1. Kết quả đánh giá độ đúng và độ lặp lại của phương pháp
3.3. Kết quả ứng dụng phân tích mẫu thực tế
3.3.1. Khảo sát ảnh hưởng của một số loại thuốc bảo vệ thực vật khác đến kết quả phân tích acetamiprid trong dung dịch AuNPs-PDADMAC
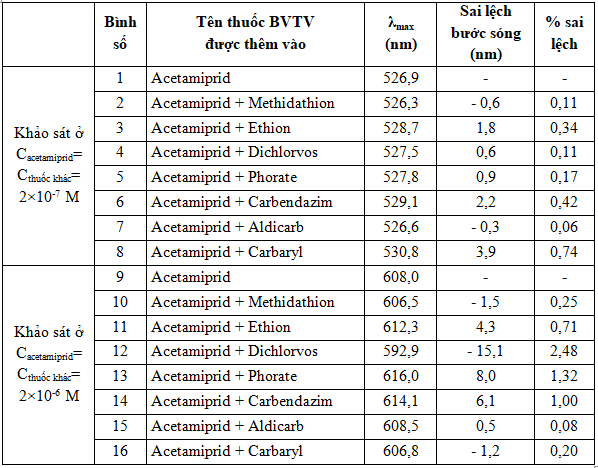
Nghiên cứu ảnh hưởng của 7 loại thuốc bảo vệ thực vật khác với nồng độ được thêm vào bằng nồng độ của acetamiprid đến sự thay đổi bước sóng cực đại của dung dịch AuNPs-PDADMAC có chứa acetamiprid. Kết quả thu được (Bảng 2) cho thấy, mức sai lệch của bước sóng hấp thụ cực đại đều nhỏ hơn 3%, do đó, có thể bỏ qua sự ảnh hưởng của các thuốc bảo vệ thực vật khác đến kết quả đo hàm lượng acetamiprid trong dung dịch AuNPs-PDADMAC.
Bảng 2. Bước sóng hấp thụ cực đại của các dung dịch AuNPs-PDADMAC chứa acetamiprid và một số thuốc bảo vệ thực vật khác.
3.3.2. Kết quả phân tích mẫu thực tế
3.3.2.1. Mẫu thuốc trừ sâu chứa acetamiprid
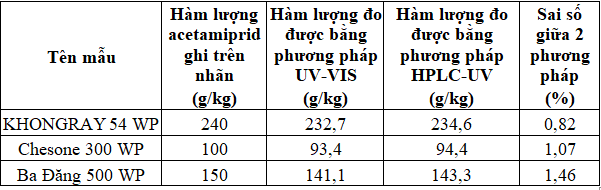
Kết quả phân tích một số mẫu thuốc trừ sâu chứa acetamiprid bằng phương pháp UV-VIS và đối chứng với phương pháp HPLC-UV (hệ thống sắc ký lỏng Waters Alliance e2695 với detector PDA) [12] được cho trong Bảng 3. Kết quả cho thấy, sự khác nhau giữa hai phương pháp không đáng kể (từ 0,82% đến 1,46%), cho thấy phương pháp nghiên cứu cho độ tin cậy cao.
Bảng 3. Kết quả phân tích một số mẫu thuốc trừ sâu chứa acetamiprid
3.3.2.2. Mẫu rau, củ được thêm chuẩn acetamiprid
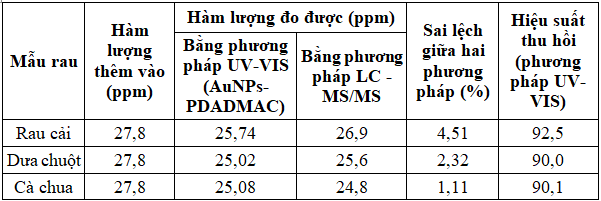
Kết quả phân tích một số mẫu trắng của rau củ quả được thêm chuẩn acetamiprid bằng phương pháp UV-VIS và đối chứng với phương pháp LC - MS/MS (hệ thống sắc ký lỏng khối phổ LC-MS/MS với hệ thống HPLC 20 AXL của Shimadzu và khối phổ ABI 6500 QQQ của Aplied Biosystem) [13] được cho trong Bảng 4. Kết quả cho thấy, sự khác nhau giữa hai phương pháp nhỏ hơn 5%. Mặt khác, hiệu suất thu hồi của phương pháp nghiên cứu đạt trên 90%, đáp ứng yêu cầu phân tích thực tế.
Bảng 4. Hàm lượng acetamiprid xác định trong mẫu rau được thêm chuẩn acetamiprid
4. KẾT LUẬN
Trong nghiên cứu này, chúng tôi đã xây dựng thành công phương pháp quang phổ hấp thụ phân tử UV-VIS sử dụng hiện tượng thay đổi tính chất plasmon bề mặt của dung dịch AuNPs được ổn định bằng PDADMAC khi có mặt chất bảo vệ thực vật acetamiprid. Phương pháp có quy trình đơn giản, ít tốn kém nhưng cho độ chính xác cao, giới hạn phát hiện và giới hạn định lượng thấp (LOD = 2,7×10-8 M, LOQ = 8,2×10-8 M). Phương pháp được ứng dụng trong phân tích mẫu thực tế là các mẫu thuốc trừ sâu chứa acetamiprid, các mẫu rau củ được bán trên thị trường cho kết quả với độ chính xác cao. Nghiên cứu góp phần đánh giá được chất lượng thuốc trừ sâu, cũng như phát hiện được lượng acetamiprid tồn dư trong các loại rau, củ được bày bán trên thị trường, góp phần vào công tác kiểm nghiệm an toàn vệ sinh thực phẩm.
Tài liệu tham khảo
2. Mohanaruban Pravinson, Selladurai Pirasath, Sivahamy Uthayakumaran, Acute poisoning with acetamiprid, a type of neonicotinoid insecticide causing severe lactic acidosis: A case report, SAGE Open Medical Case Report, 2021, 9:1-6.
3. Mohammad Faraji, Mohammadkazem Ramezani, Determination of acetamiprid, imidacloprid, and spirotetramat and their relevant metabolites in pistachio using modified QuEChERS combined with liquid chromatography- tandem mass spectrometry, Food Chemistry, 2018, 240:634-641.
4. Marinal Lopez-Garcia, Roberto Romero-Gonzalez, Marina Lacasana, Antonia Garrido Frenich, Semiautomated determination of neonicotinoids and characteristic metabolite in urine samples using TurboFlow coupled to ultra high performance liquid chromatography coupled to Orbitrap analyzer, Journal of Pharmaceutical and Biomedical Analysis, 2017, 146:378-386.
5. Weiqian Liang, Juntao Wang, Xiaohuan Zang, Wenhuan Dong, Chun Wang, Zhi Wang, Barley husk carbon as the fiber coating for the solid-phase microextraction of twelve pesticides in vegetables prior to gas chromatography-mass spectrometric detection, Journal of Chromatography Analysis, 2017, 1491: 9-15.
6. Li Ruiyi, Li Zaijun, Electrochemical detection of omethoate and acetamiprid in vegetable and fruit with high sensitivity and selectivity based on pomegranate-like gold nanoparticle and double target-induced DNA cycle signal amplification, Sensors and Actuators B: Chemical, 2022, 359:131597.
7. Xu Yan, Xingguang Su, Visual and fluorescent detection of acetamiprid based on the inner filter effect of gold nanoparticles on ratiometric fluorescence quantum dots, Analytical Chimica Acta, 2014, 852:189-195.
8. Lê Phương Thảo, Nguyễn Thị Nguyệt, Phạm Thị Ngọc Mai, Xác định paracetamol trong mẫu dược phẩm bằng phương pháp phổ hấp thụ phân tử UV-VIS sử dụng hiện tượng cộng hưởng plasmon bề mặt của dung dịch nano vàng, Tạp chí Khoa học và công nghệ nhiệt đới, 2021, 23:89-97.
9. Nguyễn Thị Hà Thu, Dương Minh Ngọc, Nguyễn Thị Thùy Linh, Phạm Thị Ngọc Mai, Sử dụng hiện tượng cộng hưởng plasmon bề mặt của dung dịch nano vàng để xác định meropenem trong mẫu dược phẩm bằng phương pháp quang học, Tạp chí Phân tích Hóa, Lý và Sinh học, 2019, 24(3):119-123.
10. Wei-Bin Tseng, Ming-Mu Hsieh, Che-Hsie Chen, Tai-Chia Chiu, Wei-Lung Tseng, Functionalized gold nanoparticles for sensing of pesticides: A review, Journal of Food and Drug Analysis, 2020, 28(4):521-538.
11. Quang Khanh Nguyen, Thi Hieu Hoang, Xuan Thanh Bui, Thi Anh Huong Nguyen, Tien Duc Pham, Thi Ngoc Mai Pham, Synthesis and appycation of polycation stabilized gold nanoparticles as a highly sensitive sensor for molecular cysteine determination, Microchemical Journal, 2021, 168:106481.
12. TCCS 07:2001 CL, Thuốc trừ sâu chứa hoạt chất acetamiprid - Yêu cầu kỹ thuật và phương pháp thử.
13. TCVN 9333:2012 Thực phẩm, Xác định dư lượng thuốc bảo vệ thực vật bằng sắc ký khí khối phổ và sắc ký lỏng khối phổ hai lần - Phương pháp QuEChERS.